|
ELEKTRON ALIŞVERİŞİ VE SONUÇLARI:
Helyum (2), neon (10), argon (18)in elektron dağılımları incelendiğinde
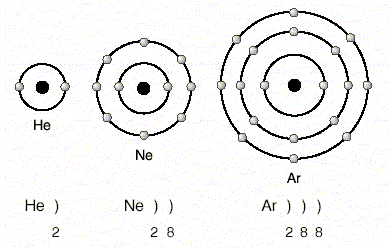
Eğer bu üç elementin birer elektronu daha olsaydı, her birinde yeni bir katman oluşacaktı. Çünkü her üçünün de en dıştaki katmanları tamamen dolu durumdadır.
1.Katmanda en çok 2 elektron bulunması durumu dublet kuralı, 2. ve 3. katmanlarda en çok 8 elektron bulunması durumu oktet kuralı olarak adlandırılır. Helyum dublet, neon ve argon oktet kuralına uyar. Oktet veya dublet kuralına uyan atomlar kararlı yapıya sahiptir.
Diğer elementler de kararlı yapıya sahip olmak isterler. Bu yüzden elektron alır veya verirler.
Son yörüngesindeki elektron sayısı az olan lityum (3), berilyum (5) gibi elementler elektron verme eğilimindedir.
Oksijen(8), flor(9) elementleri ise elektron almaya yatkındır.
Atomlar elektron alarak veya vererek kararlı yapıya ulaştıklarında artık, iyon olarak adlandırılırlar.
Nötr bir atomun elektron almış veya vermiş haline iyon denir.
Atom elektron alarak kararlı hale geçerse elektron sayısı>proton sayısı olur. Bu tür iyonlara negatif(-) yüklü iyon (anyon)denir.
Atom elektron vererek kararlı hale geçerse elektron sayısı(+)yüklü iyon (katyon)denir.
Atomlar kaybettikleri elektron sayısı kadar +yüklü, kazandıkları elektron sayısı kadar – yüklü olurlar. Not: iyon yükü =proton sayısı- elektron sayısı
Eğer iyon anyonsa sembolün sağ üst kısmına – işareti konur ve aldığı elektron sayısı yazılır. Katyonsa + işareti konur ve sayısı yazılır.
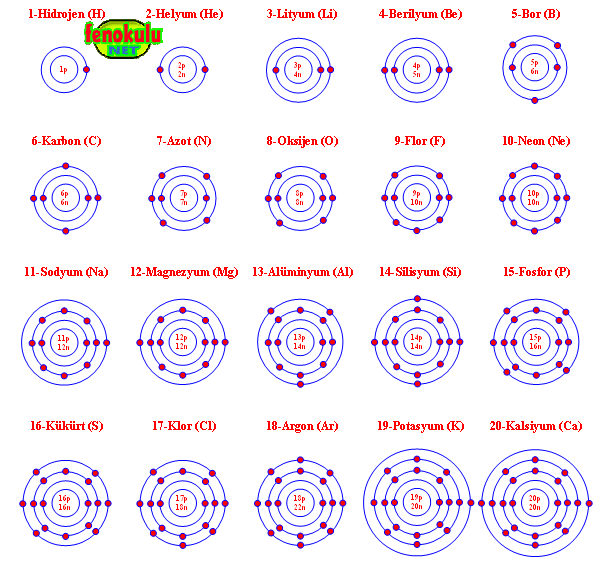
Elementlerin Atom Modelleri :
|